肺がんの薬物治療と副作用
肺がん治療に使用される3つの薬物療法
肺がんの薬物療法には、1980年代ぐらいからある細胞障害性抗がん剤、2000年代から開発されてきた分子標的薬、2015年から実際に使用されるようになった免疫チェックポイント阻害剤の3種類があります。

それぞれに特長のある作用と効果をもち、さまざまな副作用が発現します。
従来から使われている細胞障害性抗がん剤
正常な細胞は、決まった通りに分裂しながら成長し、やがて役目を終えると死滅します。ところががん細胞は、無秩序に分裂しながら成長し、死滅することなく増え続けるのです。
この無秩序に増え続けるがん細胞を死滅させるのが細胞障害性抗がん剤であります。これは、正常な細胞まで死滅させるため、副作用が発現するのです。この抗がん剤には、経口薬と注射薬があります。
現在の肺がんの薬物療法として頻繁に使用されているのが、シスプラチン※1になります。このシスプラチンを投与することで強い吐き気が副作用として発現します。
※1 カルボプラチン:点滴静注、医薬品名はパラプラチン・カルボプラチン、プラチナ製剤として有名
がんの遺伝子治療から登場した分子標的薬
分子標的薬は、医学や分子生物学の進化によって開発されたものです。分子標的薬とは、従来の抗がん剤が正常な細胞まで攻撃するのに対して、がん細胞の増殖に関係した特定のたんぱく質や遺伝子を標的に攻撃する薬剤です。つまりがん細胞だけに選択的に作用することになります。

肺がんに適応となる分子標的薬は、進行肺がんの大半を占める非扁平上皮がんの患者さんのうち、EGFR(上皮成長因子受容体)遺伝子変異※2、ALK(未分化リンパ腫キナーゼ)融合遺伝子※3、ROS1融合遺伝子※4が陽性であることです。分子標的薬は、これらの遺伝子に狙いを定め攻撃します。これらに対する分子標的薬は、EGFRチロシンキナーゼ阻害薬としてゲフィチニブ※5・エルロチニブ※6・アファニチブ※7、ALKチロシンキナーゼ阻害としてアレクチニブ※8・クリゾチニム※9であります。ROS1チロシンキナーゼ阻害は、ALKチロシンキナーゼ阻害に使われるクリゾチニムが有効とされています。
また分子標的薬は、従来の抗がん剤のような副作用が少なくなりましたが、皮膚や爪の変化、下痢、高血圧、出血などがあり重症の場合は間質性肺炎の危険性があります。
※2 EGFR遺伝子変異:がんを増殖させるためのスイッチとなり、がん細胞が限りなく増え続けます。
※3 ALK融合遺伝子:ALK融合遺伝子からできたたんぱく質があると、がん細胞が限りなく増え続けます。
※4 ROS1融合遺伝子:ROS1融合遺伝子もALK融合遺伝子と同じような作用で、遺伝子が違うだけです。
※5 ゲフィチニブ:経口、医薬品名はイレッサ、EGFRチロシンキナーゼ選択的阻害剤
※6 エルロチニブ:経口、医薬品名はタルセバ、EGFRチロシンキナーゼ選択的阻害剤
※7 アファニチブ:経口、医薬品名はジオトリフ、EGFRチロシンキナーゼ選択的阻害剤
※8 アレクチニブ:経口、医薬品名はアレセンサ、ALKチロシンキナーゼ阻害剤
※9 クリゾチニム:経口、医薬品名はザーコリ、ALKチロシンキナーゼ阻害剤、ROS1チロシンキナーゼ阻害
新しいがん治療法として登場した免疫チェックポイント阻害薬
免疫チェックポイント阻害剤という薬剤を、聞いたことのない人のほうが多いのではないでしょうか。

通常、正常な細胞から何らかの原因でがん細胞になるとき、自己免疫といわれるT細胞が攻撃してくれます。またT細胞は、がん細胞が増殖するのに対しても攻撃します。このようにT細胞は、がん細胞からわたしたちの身体を守ってくれているのです。
ところが、がん細胞にとってのT細胞は、邪魔な存在になります。そこでがん細胞は、T細胞の攻撃にブレーキをかける鍵を利用するようにしたのです。この鍵をかけられたT細胞は、がん細胞を攻撃しません。そしてがん細胞は、限りなく増殖が続けられるのです。
このときのがん細胞がもつ鍵をPD-L1と呼び、T細胞の鍵穴をPD−1と呼びます。PD−1は、ノーベル生理学・医学賞を受賞した京都大学の本庶佑特別教授が発見した分子です。
免疫チェックポイント阻害剤は、T細胞のPD−1とがん細胞のPD−L1が結合するのを阻止する薬剤です。しかし免疫チェックポイント阻害剤は、まだまだわからないところがあるため、がん細胞を免疫染色してPD−L1が多く発生していることを確認できたら使用します。
肺がんで適応になる免疫チェックポイント阻害剤は、ペムブロリズマブ※10とニボルマブ※11だけです。第1選択薬はペムブロリズマブになります。
免疫治療のイメージからは副作用が少ないものだと考えられがちです。ところがT細胞を増やし免疫力をあげることで、間質性肺炎、甲状腺機能異常、劇症Ⅰ型糖尿病、自己免疫性腸炎、重症筋無力症などの重篤な副作用が発現します。これらは、自己免疫疾患と呼ばれています。
※10 ペムブロリズマブ:経口、医薬品名はキイトルーダ、保険適応は、PD−L1陽性の切除不能な進行・再発の非小細胞肺癌
※11 ニボルマブ:経口、医薬品名はオプジーボ、保険適応は、切除不能な進行・再発の非小細胞肺癌
抗がん剤の副作用
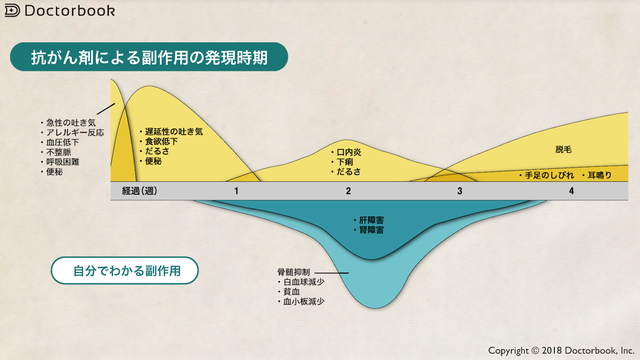
抗がん剤の副作用は、がん細胞へ攻撃ともに正常細胞も攻撃するから発生します。正常細胞は、細胞分裂によって成長し役割が終わると死滅するようにプログラミングされています。この細胞の生まれ変わりは、身体の部位によって速いところと遅いところがあります。この速度によって抗がん剤よる副作用の発現部位の順番がわかるのです。主な副作用は、吐き気、白血病減少(感染症にかかりやすくなる)、脱毛の順番になっています。
自分でわかる副作用
ü 投与日 急性の吐き気 アレルギー 血圧低下 不整脈 呼吸困難 便秘
ü 2〜7日 遅延性の吐き気 食欲低下 だるさ 便秘
ü 7〜14日 口内炎 下痢 だるさ
ü 14〜28日 脱毛 手足のしびれ 耳鳴り
検査でわかる副作用
ü 7〜14日 骨髄抑制(白血球減少・血小板減少) 肝障害 腎障害
ü 14〜28日 骨髄抑制(貧血)
副作用を対処できる時代
抗がん剤による主な副作用には、吐き気、白血球減少、だるさ、手足のしびれ、脱毛があります。このうち、吐き気や嘔吐についてはよい制吐剤が開発され、かなりの制御ができるようになりました。その制吐剤は、嘔吐中枢に働くイメンド※12、消化管の末梢神経に働くアロキシ※13などです。
あと、抗がん剤による白血球減少は、免疫力の低下から感染症にかかりやすくなります。感染症になると予後が悪くなります。最近では、白血球を上げる薬が登場してきたので、重篤な感染症を起こすことがかなり減りました。白血球を上げる薬剤は、CSF製剤※14と呼ばれています。
※12 イメンド:経口 適応症は、強い悪心、嘔吐が生じる抗悪性腫瘍剤(シスプラチン等)の投与の場合に限り使用
※13 アロキシ:静注 適応症は、強い悪心、嘔吐が生じる抗悪性腫瘍剤(シスプラチン等)の投与の場合に限り使用
※14 CSF製剤:ニューポジェン(フィルグラスチム)、ニューラスタ(ペグフィルグラスチム)、プロカイン(サルグラモスチム)など。抗がん剤投与から24時間後に注射します。
吉岡弘鎮先生からのメッセージ
進行肺がんと診断された患者さまへ、まずはいきなり諦めないで欲しいのです。その理由は、進行肺がんに対する薬物治療の選択肢が増えているからです。このような情報を患者さんとざっくばらんにしっかりと内容を伝え話し合うことで、今後のご希望や何をしたいかに合わせた最大のサポートができるのです。われわれは、患者さんにとって1番よい治療成績が得られるようにいっしょに頑張っていきます。
